Consecuencias impensadas: hoy el planeta podría deshacerse finalmente de los mosquitos, ¿pero deberíamos?
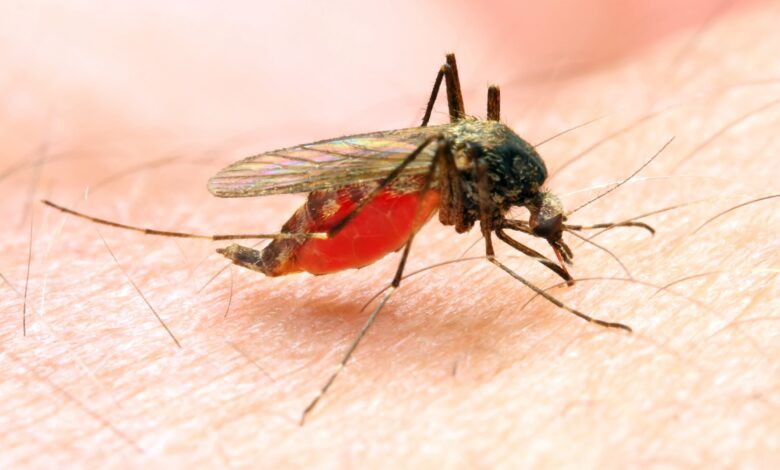
WASHINGTON.– Zumban, pican y son causa de algunas de las enfermedades más letales para la humanidad. Los mosquitos tal vez sean los animales más universalmente odiados. Si pudiéramos borrarlos de la faz de la Tierra, ¿deberíamos?
Esa pregunta ya no es hipotética: en los últimos años, los científicos desarrollaron poderosas herramientas genéticas que podrían erradicar al mosquito de una vez y para siempre.
Algunos médicos y científicos sostienen que es hora de dar ese paso extraordinario de liberar el potencial de la edición de genes para eliminar a los mosquitos y evitarles a los humanos sufrimientos como el dengue, la malaria, el virus del Nilo Occidental, y tantas otras enfermedades graves.
“Son tantas las vidas en riesgo por la malaria que queremos asegurarnos de que esta tecnología sea usada en un futuro próximo”, dice Alekos Simoni, biólogo molecular del proyecto Malaria Target, que apunta a los mosquitos transmisores de la enfermedad en el África Subsahariana.

El desarrollo de esta tecnología, sin embargo, también plantea un profundo dilema ético: ¿es aceptable exterminar intencionalmente una especie? Y de ser así, ¿en qué casos?
Algunos investigadores y especialistas en ética advierten que puede ser demasiado peligroso manipular los fundamentos de la vida misma, porque hasta los molestos y diminutos mosquitos –afirman– podrían tener suficiente valor intrínseco como para no eliminarlos.
Cómo exterminar el mosquito
El proyecto Target Malaria es uno de los esfuerzos más ambiciosos para eliminar el mosquito. El objetivo de Simoni y sus colegas es disminuir la población perteneciente al complejo Anopheles gambiae, responsables de la propagación de la mortal malaria.
En sus laboratorios, los científicos introdujeron una mutación genética que hace que las crías de mosquito hembra eclosionen sin ovarios funcionales, o sea, infértiles. Las crías macho también pueden ser portadoras del gen, pero no tienen alteraciones físicas. El concepto es que cuando los mosquitos hembra hereden el gen tanto de su madre como de su padre morirán sin tener descendencia. Mientras tanto, cuando los machos y las hembras portadores de una sola copia del gen se aparean con mosquitos silvestres, propagarán el gen aún más, hasta que no queden hembras fértiles y la población se desplome.
Simoni tiene la esperanza de que Target Malaria pueda trascender el laboratorio y liberar algunos de los mosquitos modificados genéticamente en sus hábitats naturales en los próximos cinco años. Este proyecto de investigación sin fines de lucro obtiene su financiamiento principal de la Fundación Gates, respaldada por Bill Gates, cofundador de Microsoft, y de Open Philanthropy, respaldada por Dustin Moskovitz, cofundador de Facebook, y su esposa, Cari Tuna.
El núcleo del trabajo de Target Malaria es una poderosa herramienta de ingeniería genética llamada “impulso genético”, también conocida como “genética dirigida”.
Según las reglas habituales de la genética, un progenitor tiene un 50% de probabilidades de transmitir un gen determinado a su descendencia. Pero aplicando una herramienta genética especial –denominada impulso genético– a segmentos de ADN, los científicos pueden manipular el resultado de esa “moneda al aire” y asegurarse de que un gen determinado se incluya en los óvulos y el esperma de un animal, prácticamente garantizando que sea transmitido a su prole.
A lo largo de sucesivas generaciones, esos impulsos genéticos pueden hacer que determinado rasgo se extienda a toda la población de una especie, incluso si ese gen no es beneficioso para el organismo.
De esta manera, los impulsos genéticos logran algo extraordinario: que los humanos pasemos por encima de las reglas de selección natural de Charles Darwin, que normalmente impulsan a las poblaciones de plantas y animales a adaptarse a su entorno a lo largo del tiempo.
“La tecnología nos presenta nuevas alternativas”, apunta Christopher Preston, filósofo ambiental de la Universidad de Montana. “Hace 150 años podríamos haber extinguido a fuerza de arpones o derribándolas a tiros del cielo. Pero hoy tenemos otras opciones, y la extinción de una especie podría completarse o iniciarse en un laboratorio”.
¿Hasta qué punto erradicar el mosquito?
Mientras que hay miles de conservacionistas abocados a salvar plantas y animales de la desaparición, el mosquito es una de las pocas criaturas que según el común merece la extinción. El pequeño mosquito es el animal más mortífero de la Tierra.
La tragedia humana que causa la malaria es innegable. Según la Organización Mundial de la Salud, en 2023 murieron una 600.000 personas a causa de la enfermedad, la mayoría de ellas en África.
La cifra de fallecidos es ese continente “es similar a la de estrellar todos los días dos Boeing 747 contra el monte Kilimanjaro”, señala Paul Ndebele, bioeticista de la Universidad George Washington.

Para los defensores de la genética dirigida, es fácil justificar la liberación de mosquitos modificados en países como Burkina Faso o Uganda. “Ese no es un público difícil de convencer, porque hablamos de personas que viven en una zona donde la enfermedad mata a los niños”, afirma Krystal Birungi, entomóloga de Target Malaria en Uganda. Sin embargo, Birungi señala que a veces tiene que luchar contra la desinformación, como la falsa idea de que las picaduras de mosquitos genéticamente modificados pueden dejar estériles a los humanos.
Hace poco, el Centro de Bioética Hastings, un instituto de investigación de Nueva York, junto con la Universidad Estatal de Arizona, reunieron a un grupo de bioeticistas para debatir los posibles riesgos de intentar provocar la extinción de una especie. En una investigación sobre políticas públicas publicado el mes pasado en la revista Science, el grupo concluyó que “la extinción total deliberada de una especie podría ser aceptable en algún caso, pero solo en muy raras ocasiones”.
Un candidato convincente para su erradicación total, según los bioeticistas, es el gusano barrenador del Nuevo Mundo. Esta mosca parásita que pone huevos en heridas y se alimenta de la carne, tanto de humanos como de ganado, parece tener un papel mínimo en los ecosistemas. Además, las infecciones que causa son difíciles de tratar y pueden acarrear una muerte lenta y dolorosa. Por otro lado, en el mismo informe aclaran que sería demasiado arriesgado, por ejemplo, utilizar la genética dirigida en los roedores invasores de islas remotas del Pacífico, donde diezman la población de aves nativas, dada la probabilidad no nula de que una rata o un ratón modificado genéticamente salte del barco y se extienda por todo el continente.
“En nuestras conversaciones quedó claro que no estamos a favor de rehacer el mundo para adaptarlo a los deseos humanos, ni siquiera a nivel microbiano”, indica Gregory Kaebnick, investigador principal del instituto.
La importancia de los mosquitos portadores de la malaria para los ecosistemas en general no está clara, y se investigó poco para determinar si las ranas y otros animales que se alimentan de esos mosquitos podrían encontrar otro alimento. Además, hoy los científicos debaten acaloradamente si en muchas partes del mundo no se está produciendo un “apocalipsis de los insectos” más amplio, poniendo en peligro a otras criaturas que dependen de ellos para su alimentación y polinización. “La erradicación del mosquito mediante tecnología genética puede lograr una erradicación global de una forma un poco arriesgada”, afirma Preston, quien contribuyó con Ndebele en el informe publicado en Science.
Según los autores, en cambio, los genetistas deberían poder utilizar la edición genética, las vacunas y otras herramientas no para atacar al mosquito en sí, sino al parásito unicelular Plasmodium, responsable de la malaria. Ese microorganismo invisible, que el mosquito transfiere de su saliva a la sangre de una persona al picarla, es el verdadero culpable de la enfermedad.
“Se puede eliminar la malaria sin tener que eliminar realmente al mosquito”, explica Kaebnick, y agrega que, ahora que el gobierno de Donald Trump habla despreocupadamente de la extinción de especies animales, la extinción intencional debería ser una opción solo “para especies particularmente aterradoras”.
Pero Ndebele, originario de Zimbabue, señala que la mayoría de quienes se oponen a la eliminación del mosquito “no viven en África”. Él tiene una experiencia íntima y personal con la malaria: una vez tuvo que llevar de urgencia a su hijo enfermo al hospital, cuando la enfermedad se manifestó como un episodio alucinatorio. “Estábamos en pánico. No entendíamos lo que le pasaba”, recuerda.
De todos modos, tanto Ndebele como sus colegas hablan de cautela sobre el uso de la tecnología de impulso genético.
Kaebnick dice que aunque la gente estuviera de acuerdo en eliminar todos los mosquitos del planeta –y no solo el complejo Anopheles gambiae, sino también los que transmiten otras enfermedades o simplemente pican e irritan–, sería “una empresa titánica”.
Hay más de 3500 especies conocidas de mosquitos, cada una de las cuales potencialmente necesitaría su propio impulso genético, especialmente diseñado para esa especie. Además, no hay garantía de que un impulso genético elimine una población, tal como se pretende.
Simoni coincide en que existen límites a lo que la tecnología puede hacer. El modelo proyectivo elaborado por su equipo sugiere que se lograría eliminar los mosquitos portadores de malaria solo localmente, sin eliminarlos por completo.
Los mosquitos “existen desde hace cientos de millones de años. Es una especie muy difícil de eliminar”, concluye el científico.
(Traducción de Jaime Arrambide)
WASHINGTON.– Zumban, pican y son causa de algunas de las enfermedades más letales para la humanidad. Los mosquitos tal vez sean los animales más universalmente odiados. Si pudiéramos borrarlos de la faz de la Tierra, ¿deberíamos?
Esa pregunta ya no es hipotética: en los últimos años, los científicos desarrollaron poderosas herramientas genéticas que podrían erradicar al mosquito de una vez y para siempre.
Algunos médicos y científicos sostienen que es hora de dar ese paso extraordinario de liberar el potencial de la edición de genes para eliminar a los mosquitos y evitarles a los humanos sufrimientos como el dengue, la malaria, el virus del Nilo Occidental, y tantas otras enfermedades graves.
“Son tantas las vidas en riesgo por la malaria que queremos asegurarnos de que esta tecnología sea usada en un futuro próximo”, dice Alekos Simoni, biólogo molecular del proyecto Malaria Target, que apunta a los mosquitos transmisores de la enfermedad en el África Subsahariana.

El desarrollo de esta tecnología, sin embargo, también plantea un profundo dilema ético: ¿es aceptable exterminar intencionalmente una especie? Y de ser así, ¿en qué casos?
Algunos investigadores y especialistas en ética advierten que puede ser demasiado peligroso manipular los fundamentos de la vida misma, porque hasta los molestos y diminutos mosquitos –afirman– podrían tener suficiente valor intrínseco como para no eliminarlos.
Cómo exterminar el mosquito
El proyecto Target Malaria es uno de los esfuerzos más ambiciosos para eliminar el mosquito. El objetivo de Simoni y sus colegas es disminuir la población perteneciente al complejo Anopheles gambiae, responsables de la propagación de la mortal malaria.
En sus laboratorios, los científicos introdujeron una mutación genética que hace que las crías de mosquito hembra eclosionen sin ovarios funcionales, o sea, infértiles. Las crías macho también pueden ser portadoras del gen, pero no tienen alteraciones físicas. El concepto es que cuando los mosquitos hembra hereden el gen tanto de su madre como de su padre morirán sin tener descendencia. Mientras tanto, cuando los machos y las hembras portadores de una sola copia del gen se aparean con mosquitos silvestres, propagarán el gen aún más, hasta que no queden hembras fértiles y la población se desplome.
Simoni tiene la esperanza de que Target Malaria pueda trascender el laboratorio y liberar algunos de los mosquitos modificados genéticamente en sus hábitats naturales en los próximos cinco años. Este proyecto de investigación sin fines de lucro obtiene su financiamiento principal de la Fundación Gates, respaldada por Bill Gates, cofundador de Microsoft, y de Open Philanthropy, respaldada por Dustin Moskovitz, cofundador de Facebook, y su esposa, Cari Tuna.
El núcleo del trabajo de Target Malaria es una poderosa herramienta de ingeniería genética llamada “impulso genético”, también conocida como “genética dirigida”.
Según las reglas habituales de la genética, un progenitor tiene un 50% de probabilidades de transmitir un gen determinado a su descendencia. Pero aplicando una herramienta genética especial –denominada impulso genético– a segmentos de ADN, los científicos pueden manipular el resultado de esa “moneda al aire” y asegurarse de que un gen determinado se incluya en los óvulos y el esperma de un animal, prácticamente garantizando que sea transmitido a su prole.
A lo largo de sucesivas generaciones, esos impulsos genéticos pueden hacer que determinado rasgo se extienda a toda la población de una especie, incluso si ese gen no es beneficioso para el organismo.
De esta manera, los impulsos genéticos logran algo extraordinario: que los humanos pasemos por encima de las reglas de selección natural de Charles Darwin, que normalmente impulsan a las poblaciones de plantas y animales a adaptarse a su entorno a lo largo del tiempo.
“La tecnología nos presenta nuevas alternativas”, apunta Christopher Preston, filósofo ambiental de la Universidad de Montana. “Hace 150 años podríamos haber extinguido a fuerza de arpones o derribándolas a tiros del cielo. Pero hoy tenemos otras opciones, y la extinción de una especie podría completarse o iniciarse en un laboratorio”.
¿Hasta qué punto erradicar el mosquito?
Mientras que hay miles de conservacionistas abocados a salvar plantas y animales de la desaparición, el mosquito es una de las pocas criaturas que según el común merece la extinción. El pequeño mosquito es el animal más mortífero de la Tierra.
La tragedia humana que causa la malaria es innegable. Según la Organización Mundial de la Salud, en 2023 murieron una 600.000 personas a causa de la enfermedad, la mayoría de ellas en África.
La cifra de fallecidos es ese continente “es similar a la de estrellar todos los días dos Boeing 747 contra el monte Kilimanjaro”, señala Paul Ndebele, bioeticista de la Universidad George Washington.

Para los defensores de la genética dirigida, es fácil justificar la liberación de mosquitos modificados en países como Burkina Faso o Uganda. “Ese no es un público difícil de convencer, porque hablamos de personas que viven en una zona donde la enfermedad mata a los niños”, afirma Krystal Birungi, entomóloga de Target Malaria en Uganda. Sin embargo, Birungi señala que a veces tiene que luchar contra la desinformación, como la falsa idea de que las picaduras de mosquitos genéticamente modificados pueden dejar estériles a los humanos.
Hace poco, el Centro de Bioética Hastings, un instituto de investigación de Nueva York, junto con la Universidad Estatal de Arizona, reunieron a un grupo de bioeticistas para debatir los posibles riesgos de intentar provocar la extinción de una especie. En una investigación sobre políticas públicas publicado el mes pasado en la revista Science, el grupo concluyó que “la extinción total deliberada de una especie podría ser aceptable en algún caso, pero solo en muy raras ocasiones”.
Un candidato convincente para su erradicación total, según los bioeticistas, es el gusano barrenador del Nuevo Mundo. Esta mosca parásita que pone huevos en heridas y se alimenta de la carne, tanto de humanos como de ganado, parece tener un papel mínimo en los ecosistemas. Además, las infecciones que causa son difíciles de tratar y pueden acarrear una muerte lenta y dolorosa. Por otro lado, en el mismo informe aclaran que sería demasiado arriesgado, por ejemplo, utilizar la genética dirigida en los roedores invasores de islas remotas del Pacífico, donde diezman la población de aves nativas, dada la probabilidad no nula de que una rata o un ratón modificado genéticamente salte del barco y se extienda por todo el continente.
“En nuestras conversaciones quedó claro que no estamos a favor de rehacer el mundo para adaptarlo a los deseos humanos, ni siquiera a nivel microbiano”, indica Gregory Kaebnick, investigador principal del instituto.
La importancia de los mosquitos portadores de la malaria para los ecosistemas en general no está clara, y se investigó poco para determinar si las ranas y otros animales que se alimentan de esos mosquitos podrían encontrar otro alimento. Además, hoy los científicos debaten acaloradamente si en muchas partes del mundo no se está produciendo un “apocalipsis de los insectos” más amplio, poniendo en peligro a otras criaturas que dependen de ellos para su alimentación y polinización. “La erradicación del mosquito mediante tecnología genética puede lograr una erradicación global de una forma un poco arriesgada”, afirma Preston, quien contribuyó con Ndebele en el informe publicado en Science.
Según los autores, en cambio, los genetistas deberían poder utilizar la edición genética, las vacunas y otras herramientas no para atacar al mosquito en sí, sino al parásito unicelular Plasmodium, responsable de la malaria. Ese microorganismo invisible, que el mosquito transfiere de su saliva a la sangre de una persona al picarla, es el verdadero culpable de la enfermedad.
“Se puede eliminar la malaria sin tener que eliminar realmente al mosquito”, explica Kaebnick, y agrega que, ahora que el gobierno de Donald Trump habla despreocupadamente de la extinción de especies animales, la extinción intencional debería ser una opción solo “para especies particularmente aterradoras”.
Pero Ndebele, originario de Zimbabue, señala que la mayoría de quienes se oponen a la eliminación del mosquito “no viven en África”. Él tiene una experiencia íntima y personal con la malaria: una vez tuvo que llevar de urgencia a su hijo enfermo al hospital, cuando la enfermedad se manifestó como un episodio alucinatorio. “Estábamos en pánico. No entendíamos lo que le pasaba”, recuerda.
De todos modos, tanto Ndebele como sus colegas hablan de cautela sobre el uso de la tecnología de impulso genético.
Kaebnick dice que aunque la gente estuviera de acuerdo en eliminar todos los mosquitos del planeta –y no solo el complejo Anopheles gambiae, sino también los que transmiten otras enfermedades o simplemente pican e irritan–, sería “una empresa titánica”.
Hay más de 3500 especies conocidas de mosquitos, cada una de las cuales potencialmente necesitaría su propio impulso genético, especialmente diseñado para esa especie. Además, no hay garantía de que un impulso genético elimine una población, tal como se pretende.
Simoni coincide en que existen límites a lo que la tecnología puede hacer. El modelo proyectivo elaborado por su equipo sugiere que se lograría eliminar los mosquitos portadores de malaria solo localmente, sin eliminarlos por completo.
Los mosquitos “existen desde hace cientos de millones de años. Es una especie muy difícil de eliminar”, concluye el científico.
(Traducción de Jaime Arrambide)
Gracias a una técnica genética, podrían eliminarse las especies que transmiten muchas enfermedades mortales; allí empieza el debate ético LA NACION






